来源|中山大学编辑|化学Plus
引导阅读
化疗是临床上主要的癌症治疗方法,但如何解决化疗药物的肿瘤选择性仍是化学和生物医学交叉领域亟待解决的问题。最近,基于癌细胞和正常细胞的代谢差异,中山大学化学学院毛宗万教授的团队在癌症的靶向诊断和治疗领域取得了新的进展。
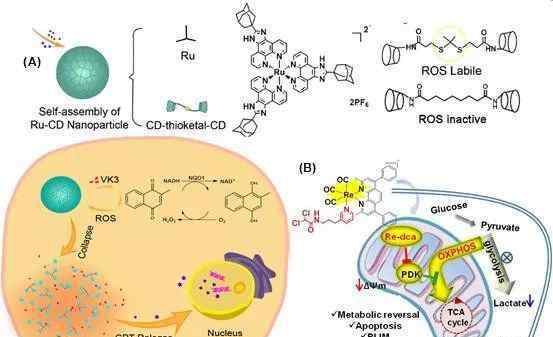
磷光金属钌配合物介导的自组装纳米系统在肿瘤组织中选择性释放化疗药物,并实时跟踪药物释放过程; Re-dca能有效逆转肿瘤细胞的有氧糖酵解代谢途径。
最近,中山大学化学学院的毛宗万教授基于癌细胞与正常细胞的代谢差异,设计了以线粒体为靶点的磷光金属铼配合物Re-dca与二氯乙酸偶联,能有效渗透并选择性地在线粒体内积累,通过抑制丙酮酸脱氢酶激酶的活性,诱导肿瘤细胞的代谢逆转,从而像正常细胞一样逆转有氧糖酵解到氧化磷酸化的代谢途径。这种靶向调节肿瘤代谢途径的策略,对正常细胞的作用很小,从而实现对肿瘤细胞的选择性杀伤,抑制转移和侵袭。
为了进一步提高药物的肿瘤选择性,毛宗万教授的团队还设计开发了一种磷光金属钌配合物介导的自组装纳米诊疗系统,该系统能够有效包裹抗癌药物喜树碱和维生素K3,诱导维生素K3的酶催化氧化还原循环与肿瘤组织中自组装纳米系统ROS反应崩解之间的级联正反馈,从而在肿瘤部位选择性释放化疗药物。
这种策略在细胞和活体水平上实现了对肿瘤的选择性杀伤,对正常组织无毒副作用。随着药物在活体中的释放,自组装系统的磷光逐渐亮起,可以指导治疗时药物释放的时间、位置和效率,对开发多模式协同治疗的癌症诊疗系统具有指导意义。
这两项研究成果已连续发表在著名的生物医学杂志《生物材料》上。它们是“通过无热铼-DCA会聚的癌细胞代谢的靶向逆转和荧光场景寿命成像,生物材料,2018,176,94-105”和“基于维生素k3介导的ROS再生反馈和体内可视化药物释放的癌症特异性化疗策略,生物材料,2018,185,73-85”。论文第一作者为杨静博士和2016级博士生杨刚博士,合著者为曹干博士和毛宗万教授。
以上研究工作得到了国家973项目、国家重点项目、国家自然科学基金、广东省自然科学基金和广州市科技计划项目的资助。
论文链接:
https://doi.org/10.1016/j.biomaterials.2018.08.065
https://doi.org/10.1016/j.biomaterials.2018.05.040
1.《BIOMATERIALS 《Biomaterials》中山大学毛宗万教授团队在肿瘤靶向诊疗领域取得新进展》援引自互联网,旨在传递更多网络信息知识,仅代表作者本人观点,与本网站无关,侵删请联系页脚下方联系方式。
2.《BIOMATERIALS 《Biomaterials》中山大学毛宗万教授团队在肿瘤靶向诊疗领域取得新进展》仅供读者参考,本网站未对该内容进行证实,对其原创性、真实性、完整性、及时性不作任何保证。
3.文章转载时请保留本站内容来源地址,https://www.lu-xu.com/guoji/1668388.html