根据国际糖尿病联盟的数据,中国已经成为糖尿病患者人数最多的国家。随着糖尿病普及率的不断提高,降糖药物将在中国形成巨大的市场规模。预计2028年将达到1739亿元。
1.降糖药物的市场规模
近年来,随着老龄化、城市化和肥胖的加速,世界糖尿病患病率逐年上升。目前,糖尿病已经成为一个全球性的问题,将给各国的医疗体系带来巨大的压力,降低生产力,减缓经济增长,特别是给贫困家庭带来灾难性的后果。2017年糖尿病患者人数将达到4.249亿,国际糖尿病联盟预测2045年糖尿病患者人数将达到6.286亿。数据显示,2017年,中国糖尿病患者人数达到1.144亿(20-79岁),居世界首位。
图1:2045年全球各地区糖尿病患者数量预测
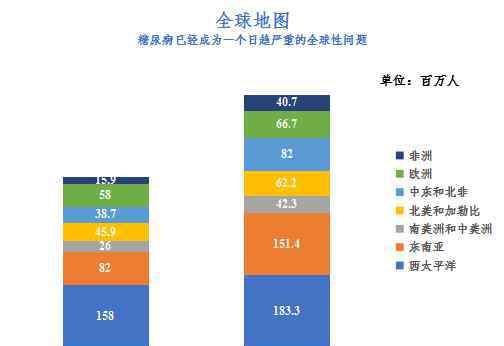
国际糖尿病联盟地图(IFD)
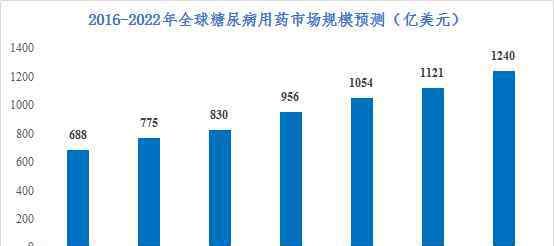
据统计,2017年全球糖尿病市场已超过700亿美元,2022年将达到1240亿美元。在糖尿病患者数量最多的中国,乔斯特·沙利文预测,抗糖尿病药物市场将从2017年的512亿元增长到2028年的1739亿元
1亿元,复合年增长率11.8%。
图2:2016-2022年全球糖尿病药物市场规模预测
2.国内降糖药物上市公司
目前,欧美企业在糖尿病药物市场占据主导地位,诺和诺德、赛诺菲、礼来、默克、阿斯利康、强生、诺华、拜耳等巨头占据80%以上的市场份额。然而,由于药品市场巨大,国内许多上市公司都在积极发展这一领域,注重布局。
2.1.通化东宝:国内领先的胰岛素企业
2017年,通化东宝实现营业收入254532.5万元,同比增长24.75%;实现利润总额97298.18万元,同比增长28.20%。
2.1.1.初级糖尿病市场潜力巨大
通化东宝作为国内胰岛素领域的龙头企业,在该领域发展了十多年,形成了完整的营销渠道优势和品牌优势。目前是国内基层二代胰岛素市场最完善的企业。与外资企业相比,它在基层渠道上具有更广泛的优势,覆盖3000多家县级医院,在基层医生中享有良好的声誉。
2.1.2.有丰富的糖尿病产品储备
糖尿病药物研发储备全面,涵盖胰岛素类似物、GLP-1受体激动剂和口服降糖药。
表1:通化东宝正在开发降糖药物项目
R&D项目
R&D(注册)阶段
进展情况
甘精胰岛素
申请生产报告
它于2017年10月宣布生产,目前正处于核查和审查阶段。
门冬胰岛素
三期临床
门冬胰岛素和门冬胰岛素注射:数据锁定已完成,预计2018年完成总结报告并申报生产;诺和锐30注射液:目前正在各个中心申请伦理学,预计2018年上半年全面上线;门冬胰岛素50注射液:临床研究正在进行中。
膳食胰岛素
已经通过临床试验
现在正处于临床试验的准备阶段。
胰岛素lispro
临床接受
目前正在审查中。
人胰岛素样肽-1类似物
临床接受
目前正在审查中。
临床应用前的工作
完成三批临床应用中试生产,全面开展质量研究、药效学药代动力学研究和药物安全性评价。
瑞格列奈二甲双胍片
仿制药一致性评估正在启动
瑞格列奈二甲双胍片的一致性评价重新开始,生物等效性研究计划于2018年完成。
瑞格列奈
生物等效性研究已经完成
生物等效性研究已经完成,相关数据处理正在进行中。
琥珀酸曲格列酮原料药和片剂
已经通过临床试验
对生物等效性进行了系统研究。
磷酸西格列汀原料药和片剂
该项目的所有药物研究都已完成
生物等效性记录已完成,生物等效性预实验已完成。各项指标与原研究相似。
西格列酮二甲双胍。
该项目的所有药物研究都已完成
生物等效性记录已完成,生物等效性预实验已完成。各项指标与原研究相似。
通化东宝2017年年报
甘精胰岛素于2017年10月宣布生产,目前正处于核实和审查阶段;门冬胰岛素注射液,至今已临床完成,现正在定稿封存;诺和锐30注射液:目前正在各个中心申请伦理学,预计2018年上半年全面上线;门冬胰岛素50注射液:临床研究正在进行中;胰岛素lispro和利拉鲁肽已被宣布为IND。丰富的产品线陆续上市后,有望充分发挥公司的渠道优势,实现协同增效。
2.2.韩宇制药:多肽药物空增长巨大
2017年,汉宇药业实现营业总收入124623.35万元,同比增长45.75%;上市公司股东应占净利润329,721,400元,同比增长12.95%。
2.2.1.对利拉鲁肽原料药的需求激增,汉宇制药成为稀缺目标
汉宇制药的多肽业务具有领先的R&D优势和高技术壁垒,这在国际上得到广泛认可。目前正处于利拉鲁肽仿制药申报的黄金时期。2017年,全球销售收入增长16%,达到38亿美元。
目前世界上能提供这种多种API的公司只有四家。汉宇药业凭借原料药认证优势,积极推进海外制剂ANDA申报,并与注射笔制造商BD公司合作,增加利拉鲁肽原料药和制剂申报销售的竞争优势。总的来说,海外肽制剂将成为汉宇制药未来的一个重要发展方向。
表2:汉宇制药正在研究降血糖药物
R&D项目
R&D(注册)阶段
进展情况
艾塞那肽和艾塞那肽注射液
申请生产
正在审查
利拉鲁肽和利拉鲁肽注射液
申请生产
拿临床披肩,进行临床试验
乙酸扁素及乙酸扁素注射液
临床试验
进行临床试验
甲磺酸溴克罗齐片(溴麦角环肽)
进口注册申请临床
获得临床批准并进行临床试验
汉宇制药2017年年报
2.3.华东医药:口服降压药龙头企业
华东医药2018年3月30日发布的最新2017年年报显示,营业收入278亿元,同比增长9.66%;上市公司股东应占净利润17.8亿元,同比增长23.01%。
2.3.1.华东医药卫生继续享受阿卡波糖药物红利
阿卡波糖是我国治疗2型糖尿病的一线药物。阿卡波糖是一种口服降糖药,占国内市场近30%,居国内口服降糖药市场首位。阿卡波糖已被列入2012年版基本药物目录。华东医药卡波姆的菌种和生产工艺与拜占庭接近,比拜占庭有价格优势。在基本药物招标方面,百糖平出于价格维持的考虑,选择了放弃部分省市招标,而华东医药则改为进口,市场份额不断攀升。2015年,华东医药在重点医院的市场份额为24%,而卡布平在2015年带来了12亿元的营收,同比大幅增长38.9%。此外,华东制药已与新药研究所达成协议,获得阿卡波糖咀嚼片,有利于进一步提升原有卡波平的附加值,巩固其市场份额。
2.3.2.降糖药物的快速分发
近年来,华东医药加快了降糖药物布局,利拉鲁肽已开始一期临床试验,进展在国内领先;同时引入口服GLP-1小分子制剂TTP273,构建GLP-1类似物领域的注射+口服管道。其他布局管道包括DPP-4抑制剂(推出1类新药HD118,2018年1月批准在中国临床使用)、SGLT-2抑制剂(模仿卡格列奈和卡格列奈二甲双胍,批准临床使用)和胰岛素类似物(地特胰岛素已报告临床使用,门冬胰岛素和胰岛素在临床使用前脱胶)。
表3:华东医药正在开发降糖药物
R&D项目
R&D(注册)阶段
进展情况
TTP273
完成研究筛选
从美国引进,目前处于国内技术转移和临床前研究阶段
HD-118及其胶片
已获得国内临床认可
进行一期临床试验
利拉鲁肽
受让方获得临床批准
一期临床试验已经开始
吡格列酮和二甲双胍片(15/850毫克)
获得临床批准
准备临床样本,开展临床试验
卡格列奈和片剂
获得临床批准
临床样本已经准备好,临床试验已经开始
黄芪甲苷及其片剂
获得临床批准
临床样本已经准备好,临床试验已经开始
复方卡格列奈二甲双胍片
获得临床批准
准备临床样本并开始临床试验
西格列汀二甲双胍复方片
已完成商务文件归档
铍试验正在进行
膳食胰岛素
申报临床
2017年底临床宣布
门冬胰岛素
完成研究筛选
临床前研究
Degu胰岛素
完成研究筛选
临床前研究
华东医药2017年年报
2.4.恒瑞医药:中国创新药物的龙头企业
2017年营业收入138.36亿元,同比增长24.72%,上市公司股东应占净利润32.17亿元,同比增长24.25%。
2.4.1.糖尿病管道布局丰富
糖尿病领域是恒瑞医药近年来重点布局的领域,将迎来一个又一个的收获期。在糖尿病研发管道中具有巨大潜力的品种包括:亨格列金(SGLT-2抑制剂,三期临床,潜力巨大)、口服GLP-1类似物(临床应用,潜力巨大)、瑞格列汀(DPP4抑制剂,三期临床,有一定潜力)、呋塞米(GPR40激动剂,一期临床应用)、长效胰岛素(临床应用)
表4:恒瑞医药正在研究降血糖药物
R&D项目
R&D(注册)阶段
亨格列京
三期临床
口头GLP-1
申报临床
亨格列汀
三期临床
芙蓉花;芙蓉花
一期临床
长效胰岛素
申报临床
恒瑞医药2017年年报
2.5.李赣制药(首次公开募股将成功):国内领先的胰岛素类似物企业
2014-2016年和2017年1-6月,李赣药业分别实现营业收入9.27亿元、12.2亿元、17.71亿元和9.8亿元;同期净利润分别为3.05亿元、4.47亿元、7.7亿元和3.71亿元。
胰岛素lispro是李赣制药的主要降糖药物,由李赣制药开发,2007年在中国上市。其价格比同类进口产品低20%左右,显著减轻了糖尿病患者的医疗负担。近年来,根据公司招股说明书,2013年、2014年和2015年的销售额分别为833万元、1231万元和1864万元,增长率保持在50%以上。此外,李赣制药有限公司也在积极开发各种降血糖药物。
表5:李赣制药正在研究降血糖药物
R&D项目
进展情况
门冬胰岛素30注射液
在注册审查过程中,
门冬胰岛素注射液
等待临床验证
精子重组人胰岛素注射液(30R预混)
在注册审查过程中,
纯蛋白锌重组胰岛素lispro混合注射液(50R)
一期临床准备
门冬胰岛素50注射液
一期临床准备
甘精胰岛素注射液(美国)
三期临床准备
李赣制药2017年年报
1.《快速降糖药 国内降糖药市场情况》援引自互联网,旨在传递更多网络信息知识,仅代表作者本人观点,与本网站无关,侵删请联系页脚下方联系方式。
2.《快速降糖药 国内降糖药市场情况》仅供读者参考,本网站未对该内容进行证实,对其原创性、真实性、完整性、及时性不作任何保证。
3.文章转载时请保留本站内容来源地址,https://www.lu-xu.com/fangchan/1173372.html


