2月12日,博瑞Bio发布公告称,已生产出remdesvir原料药,remdesvir制剂的批量生产正在进行中。
此前的“专利纠纷”之后,伦德西维尔再次成为新闻焦点。
2月12日,博锐生物医药(苏州)有限公司(以下简称“博锐生物”)发布公告称,积极响应国家抗击新型冠状病毒(2019-nCoV)疫情的号召,近日成功仿制开发了瑞德西韦原料药的合成工艺和制备工艺。该公司已经生产了大量的原材料,并正在进行大量生产。
随后,博瑞药业秘书长王表示:“我们今天已经开始生产制剂,第一批制剂大约一周就可以生产出来。我们不会在国家发大财,主要是给国家提供这种药治疗病人。”
什么时候有?
根据公告,如果该药物要上市,需要跨越几个门槛:
1.博瑞生物目前只是仿制原料,制剂的批量生产还在进行中。至少要做一些药物研究,比如稳定性试验,才能完成制剂研发。
2.完成制剂研发后,需要经过药物临床试验、药物审批等多个环节。
3.Gilead的专利不能绕过。如果博瑞Bio的Remdesivir最终转化为产品并投放市场,需要得到Gilead作为专利权人的授权;
这并不是说我们怀疑我国医药公司的技术和国家紧急审批的能力。面对疫情,我们有各种手段缩短时间,提前上市,造福患者。
然而,专利壁垒在短期内是无法逾越的。
第一,Gilead原有的研究工厂还在进行三期临床试验。如果有效的话,基列德会尽快上市,因为疫情急,时间不等人。就算价格再高,也得用。
第二,Gilead的原创研究产品没有上市,也没有收回在R&D的投资,所以不太可能提前授予专利。
所以,即使药物被成功复制,在正式上市之前还有很多未知,远水解永远不会带来近渴。
但是,不能说模仿没有意义。
早期模仿的意义
虽然疫情当前,近期不太可能上市,远水解也绝不会近渴,但该药的仿制还是有非常积极的意义:
1.这种仿制药的研发旨在响应国家号召,储备战略技术。如果在Remdesivir的临床试验有效,可以有效解决Gilead的产能不足或价格偏高的问题。
如果能掌握核心技术,那就加强了我国的筹码。基列价格飙升是可以避免的。
如果国家对药品专利实施强制许可,Remdesivir作为技术储备,面对重大情况也可以独善其身。
关于药品专利的“强制许可”,我国有相关法律法规:
专利法第四十九条规定,在国家处于紧急状态或者非常情况下,或者为了公共利益的目的,国务院专利行政部门可以对发明专利或者实用新型专利的实施给予强制许可。
《专利法》第五十条规定,为了公共卫生的目的,国务院专利行政部门可以向符合中华人民共和国参加的有关国际条约的国家或者强制许可的地区制造、出口专利药品,实行强制许可。
但“强制许可”至今未被使用。
2.展示肌肉,博瑞生物是上市公司,并宣布凭借其在开发高端原料药和特殊注射剂方面的技术积累,对资本市场有利。
3.通过正常的审批渠道获得Gilead的专利许可并正常上市也不是不可能。
4.吉利将博瑞生物列为“remdesvir”API供应商,这种合作也是可能的。因为基列德的声明提到要解决产能和原料药供应的问题。
5.企业曝光度增加,免费广告。
同时,博瑞Bio还强调“公司将Remdesivir的仿制研发视为自己的社会责任。如果该产品能够获准上市,将主要通过疫情期间的捐赠提供给相关患者。”
临床进展
伦德西韦是一种被谐音称为“人民的希望”的抗病毒药物,已于2月6日在武汉金银潭等一线医院开始临床试验。
Remdesivir的制造商Gilead明确表示,研究药物是免费提供的。

2月6日,第一个接受者是一名68岁的男性危重患者。
这个计划已经调整过多次了
此前,根据计划,试验将从2月3日开始,总样本量为270例,将纳入轻中度新冠肺炎肺炎患者。
2月5日,据伦德西韦临床试验项目负责人、中日友好医院副院长曹斌教授介绍,按照计划,将有308例轻、中度疾病患者和453例重度疾病患者纳入试验,共纳入761例患者,采用随机、双盲、安慰剂对照的方法进行试验。
整个临床试验在4月底结束。因为是双盲,医生和病人都不知道是用安慰剂还是药物。只有当失明被发现时,他们才知道结果。

用于临床试验的药物在网上流传
“我对伦德西维尔抱有很大希望。”
2月5日,王晨院士在回答白严嵩的提问时说:“根据之前的研究结果,我们对伦德西韦抱有很大的希望,其他药物包括中药还需要进一步的临床观察才能确定其疗效。特别提醒大家的是,个别药物的有效性不是科学结论,必须进行临床试验。”
中国科学院武汉病毒学研究所/生物安全科学研究中心与中国军事科学院军事医学研究所国家应急药物工程与技术研究中心联合开展的研究表明,2019年新型冠状病毒(2019-nCoV)抑制药物筛选取得重要进展。发现Remdesivir、GS-5734)和氯喹能在细胞水平上有效抑制新型冠状病毒对Vero E6细胞的感染,其在人体内的作用有待临床检验。
remdesvir(EC50 = 0.77 μm;半细胞毒性浓度cc 50 >:100 μm;选择指数si >: 129.87)
病毒感染在低微摩尔浓度下被有效阻断,并表现出高选择性指数SI。
1月31日,权威医学期刊《新英格兰医学杂志》(NEJM)在网上发表了几篇关于新型冠状病毒(2019-nCoV)病例的论文,其中一篇介绍了美国首例确诊病例的诊疗过程和临床表现。
这篇论文引起了公众的关注,因为有一种药物有立竿见影的效果:患者在住院第七天晚上开始使用Remdesivir这种药物,第二天发烧就下降了(体温从第一天的39.4摄氏度下降到第二天的37.3摄氏度),症状明显减轻!

美国第一位患者,中国人,1月15日从武汉回到美国,两天后开始发烧。1月20日确诊住院,住院后用了很多药,但还是发烧。住院第七天晚上,用了remi vir(remdesvir)的药。结果第二天就退烧了,各种症状都好了。到1月30日,患者只出现咳嗽症状,逐渐轻微。
据CNN报道,病人已经出院。
红色四维是“利巴韦林”的第二代
根据公共信息,利巴韦林,也称为利巴韦林,于1986年被批准用于临床。它是一种广谱抗病毒药物。由于对呼吸道合胞病毒(RSV)有抑制作用,利巴韦林主要用于呼吸道合胞病毒引起的病毒性肺炎和支气管炎。曾是2003年抗击非典的明星药。
魏毅博士:瑞西韦其实是“利巴韦林”的第二代。它们的作用机制是一样的。从结构上看,Remdesivir更稳定,推测其作用更强。剂量要小,体内分布更理想。理论上,大剂量的利巴韦林也应该是有效的。
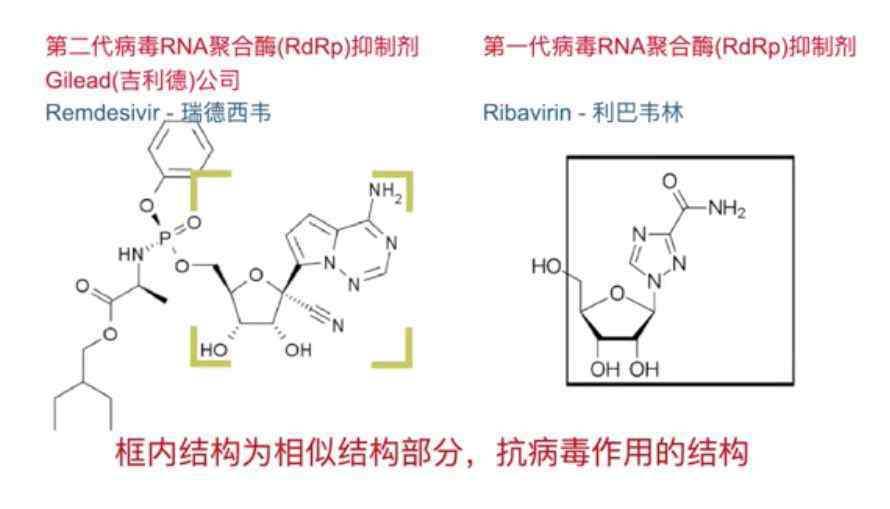
两者的结构式“母核”相似
专利纠纷
Gilead CEO在Remdesivir一案中对专利纠纷做出回应:它会保护专利,但不会介入纠纷,病人第一。
2月5日,在武汉病毒公司宣布抗病毒药物Remdesivir的专利后,Gilead Science的全球首席执行官丹尼尔·奥戴(Daniel O'Day)在一次公司会议上回应了这个漩涡中的“专利纠纷”。
当有人问基列德将如何处理武汉病毒宣布的伦德西韦专利时,丹尼尔·奥戴说:
“目前专利不是我们主要关心的问题。我问过负责专利的同事。就像贾里德的其他药物一样,我们已经在世界各地申请了包括冠状病毒在内的化合物和专利。我们不会介入这个专利问题,我们会想办法帮助患者,当然我们会用其他方式保护我们的知识产权,但患者是第一位的。”
《中国科学》杂志采访的一位相关知情人士透露,专利申请是“押一匹马”,是为了保护自己的利益。目前正在进行临床试验,无论试验结果是否证明Remdesivir有效,我们都要申请这个专利。
最后,我们期待“人民的希望”Remdesivir在临床上有好的表现,不要让人民的希望落空。
关于滴度
Drugdu滴定度平台——全球跨境医疗贸易B2B电商平台。为您提供可靠的医药和设备外贸知识,帮助您的产品走向大海,走向世界。加小滴Drugdu2,了解更多医药贸易。
1.《雷德西韦 硬核!瑞德西韦被仿制》援引自互联网,旨在传递更多网络信息知识,仅代表作者本人观点,与本网站无关,侵删请联系页脚下方联系方式。
2.《雷德西韦 硬核!瑞德西韦被仿制》仅供读者参考,本网站未对该内容进行证实,对其原创性、真实性、完整性、及时性不作任何保证。
3.文章转载时请保留本站内容来源地址,https://www.lu-xu.com/guoji/1289181.html












