3月18日,中国医科大学转化医学研究所曹流课题组在《Embo杂志》(if: 11.227)上发表了题为“ATM-chk2-beclin 1轴促进自噬维持氧化应激下ROS稳态”的研究论文。

本研究探讨了葡萄糖饥饿和缺氧应激细胞中活性氧引发的DNA损伤与自噬的关系。揭示了ROS-ATM-CHK2-Beclin 1轴介导的代谢应激触发自噬的新方式,最终证明代谢应激触发的自噬可以通过清除受损线粒体维持细胞内环境稳定。
ROS不仅是维持细胞生命活动的第二信使,也是细胞氧化应激损伤的根源。组织缺血后再灌注过程中产生的过量活性氧是心肌梗死和中风等缺血性疾病死亡的主要原因。揭示代谢应激下维持活性氧稳态的途径和分子机制,可为相关疾病的预防和治疗提供重要的科学依据。
自噬是真核细胞进化中高度保守的细胞内分解代谢途径。自噬通过双层膜结构包裹受损的生物大分子和细胞器,并将其转运至溶酶体进行降解和消除,从而维持细胞的稳态。
研究表明,自噬的缺乏会导致细胞中活性氧水平的增加。在各种应激刺激下,ROS可以作为细胞内信号分子激活自噬,提示自噬可能在维持ROS稳态中发挥重要作用。然而,活性氧触发自噬的途径和自噬调节活性氧稳态的机制仍不清楚。
这项研究证实,当细胞中活性氧水平增加时,ATM/CHK2途径被激活,磷酸化水平增加。活化的CHK2磷酸化自噬途径相关蛋白Beclin 1的Ser90/ Ser93,阻碍Beclin 1和Bcl-2的结合,释放磷酸化的Beclin 1,从而诱导自噬,通过降解受损的线粒体维持细胞的稳态。
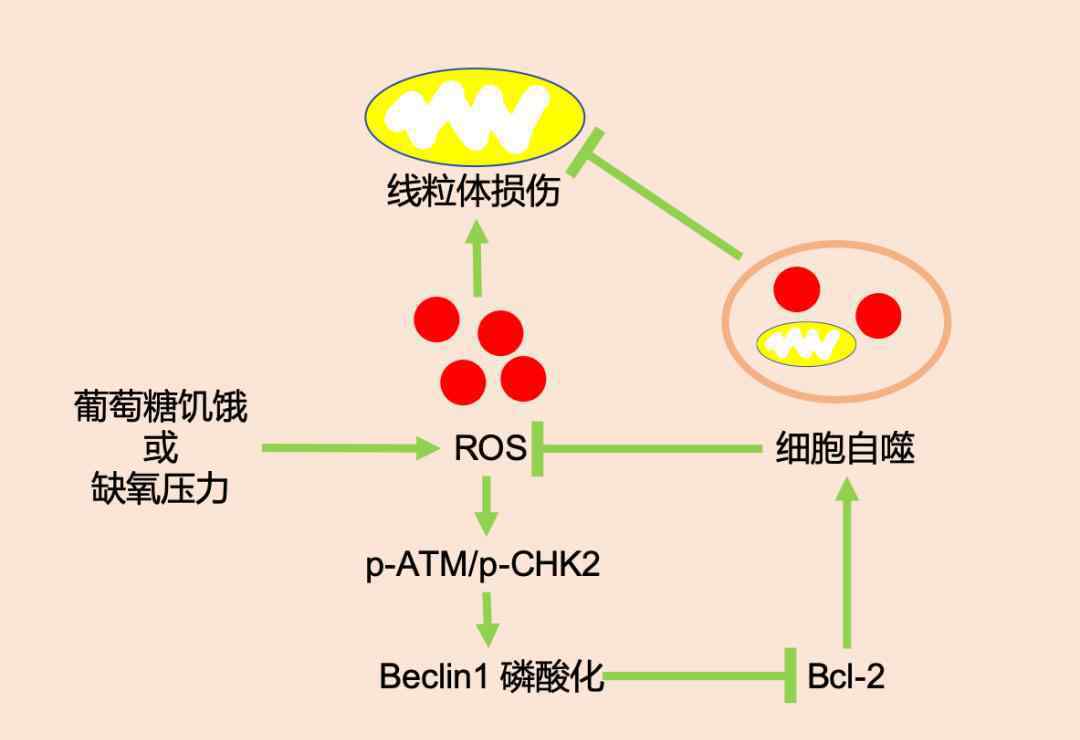
ROS-ATM-CHK2-Beclin 1轴介导的自噬指征
此外,该研究还在小鼠模型中证明了与CHK2-Beclin 1通路相关的自噬可能用于减轻缺血性中风引起的细胞死亡。
中国医科大学转化医学研究所副研究员郭奇强是本文的第一作者,基础医学院转化医学研究所曹流教授是本文的通讯作者。
合生素基因为自噬的研究提供了一个双标记的慢病毒载体(GFP-mCherry-LC3)。
点击阅读原文,直接进入原链接
1.《曹流 【学术前沿】中国医科大学曹流课题组揭示 DDR 通路 ATM-CHK2 调控细胞自噬维系氧化应激压力下 ROS 稳态新机制》援引自互联网,旨在传递更多网络信息知识,仅代表作者本人观点,与本网站无关,侵删请联系页脚下方联系方式。
2.《曹流 【学术前沿】中国医科大学曹流课题组揭示 DDR 通路 ATM-CHK2 调控细胞自噬维系氧化应激压力下 ROS 稳态新机制》仅供读者参考,本网站未对该内容进行证实,对其原创性、真实性、完整性、及时性不作任何保证。
3.文章转载时请保留本站内容来源地址,https://www.lu-xu.com/yule/1250282.html