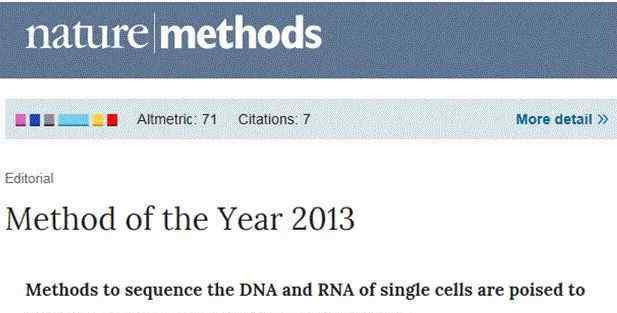
2011年,“自然方法”使单细胞测序成为当年值得期待的技术之一目前,单细胞测序已被广泛用于研究肿瘤细胞的异质性、发现新的突变位点、克隆肿瘤细胞的进化机制以及识别相关的新生物标志物。其中,在罕见肿瘤细胞(CTC细胞和弥漫性肿瘤细胞)的早期检测和监测中的应用有助于肿瘤的个性化和精确治疗。你真的理解这么热的单细胞测序吗?[文末有好处];2013年1月,《科学》杂志将单细胞测序列为当年最值得关注的六大领域之首;2014年1月,《自然方法》将单细胞测序列为2013年最重要的方法学进展,并指出《自然》系列发表的单细胞测序文章在2013年大爆发图1:自然官网。近三年来,连续发表数百篇高分文章,呈现井喷状态。以下是硬核干货。建议收藏。
单细胞测序:最受关注的领域之一
[3]
 [4]
[4]
[5]
第一个问题:分离单个靶细胞的三种方法
单细胞测序的首要问题是如何分离单个靶细胞。目前主要的单细胞分离方法有有限稀释法、显微操作法和流式细胞术。
有限稀释法是一种传统的方法,主要是使一定体积的悬浮液理论上只含有一个细胞,然后用移液管吸收相应体积的细胞悬浮液,从而获得单细胞。这种方法不需要特殊设备,目前仍被广泛使用。但是这种方法依赖于梯度稀释计算,不是直观的单细胞分离。因此,实际操作中的效率仅为20%左右,并且存在大量的空白色或多单元。
相比之下,显微操作是一种可以直接观察单细胞的方法。这种方法可以精确控制单细胞的摄取和释放,但对实验操作要求较高,不利于大规模操作。
另一方面,荧光激活细胞分选(FACS)可以大规模获得单细胞样品。在该方法中,通过使用流式细胞术借助于细胞表面标记来分选特定的细胞群或单细胞。虽然这种方法需要特殊的设备,而且细胞消化和分选的过程会对细胞状态产生一定的影响,但这种方法的效率和准确度高,标准统一,有利于不同实验室实验研究的比较[[6]。

图2:来源郝波生物
有时我们可能需要根据样本的具体情况(如何根据不同的情况选择合适的方法可能是用户感兴趣的)结合上述方法来获得单个细胞。此外,一些新方法的出现也为单细胞基因组学研究提供了便利。
意大利硅生物系统公司的DEPArray系统可以通过对细胞施加非均匀电场并结合形态学信息,从复杂的异质样品中识别和捕获单细胞。整个过程没有物理接触或摩擦,保持了细胞活性,与各种细胞悬液兼容,还可以处理穿刺和组织活检样本[7]。
美国Fluidigm公司的C1单细胞自动制备系统虽然不能对单细胞成像,但大大提高了自动化水平。该系统基于创新的微流控技术,首先自动分离96个单细胞,然后在芯片上进行细胞裂解、RNA反转录和预扩增。从单细胞制备到cDNA合成和扩增,整个过程实现了前所未有的自动化和规模化[7]。但是在细胞群体中隔离是罕见的(
对于转录水平的分析,不仅要获得单细胞,还要尽量减少对细胞状态的影响。最近,一些学者对非自然条件下的“推断生物学”表示怀疑,因为大多数关于基因表达变化的知识都是从培养细胞进行的研究中获得的。因此,他们开发了一种前所未有的方法——体内转录组分析(TIVA)[9],这种方法可以从活组织的单细胞中捕获基因,而不会对周围组织造成损害。

图3: TiVA技术原理[9]
单细胞扩增技术的过去
最早的方法出现在2009年,即唐的方法[1]。石英-序列法实际上是对唐方法的优化,进一步减少了扩增副产物的产生,简化了实验过程[10]。在CEL-seq中,用IVT代替聚合酶链反应进行扩增。第一种基于SMART的方法被称为(单细胞标记的反向转移,STRT),但只有转录物的5’端可以测序[11]。后面出现的Smart-Seq[12]和Smart-Seq2[13]可以使转录物全长测序,有成熟的商业试剂盒,目前应用广泛。

图4:来源郝波生物
万能:单细胞RNA测序的六个应用方向
多组学测序,整合研究
生命现象的发生和调控过程极其复杂,涉及到肿瘤等复杂疾病发生发展过程中基因组、转录组和表观遗传学的变化和调控。在大数据时代,结合多组学数据的多组学研究是一大趋势。多组学研究可以把握疾病的整体变化过程,为研究肿瘤调节机制和精密医学提供全面的解决方案。虽然在同一细胞中对基因组、转录组和甲基化进行测序非常困难,但已经开发了一些方法。

关于单元格组的注释
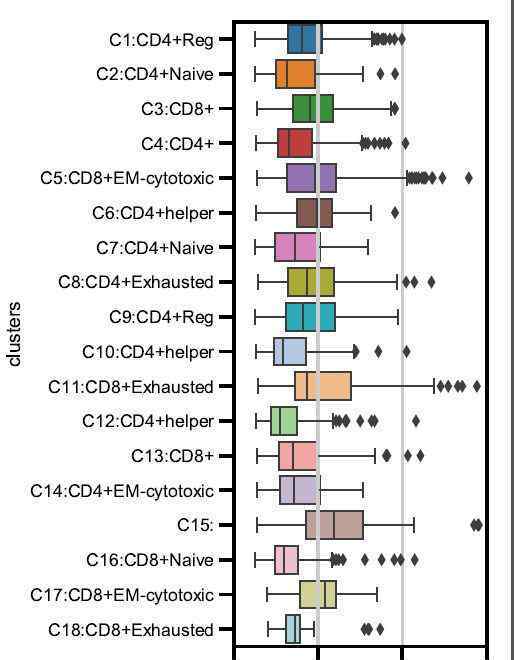
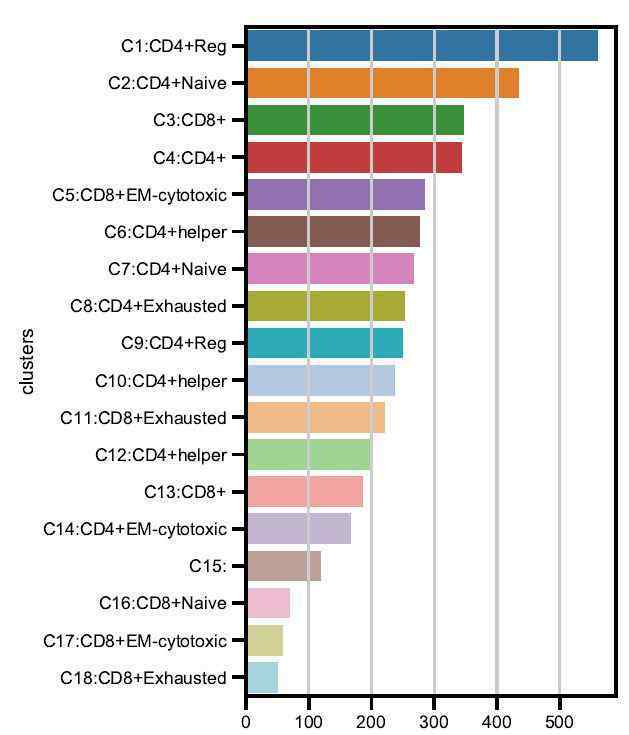
不同簇中转录物表达丰度的分布统计和不同簇中细胞数量的统计

标记基因分析

伪时间线分析

不同患者各组转录表达丰度和细胞数统计
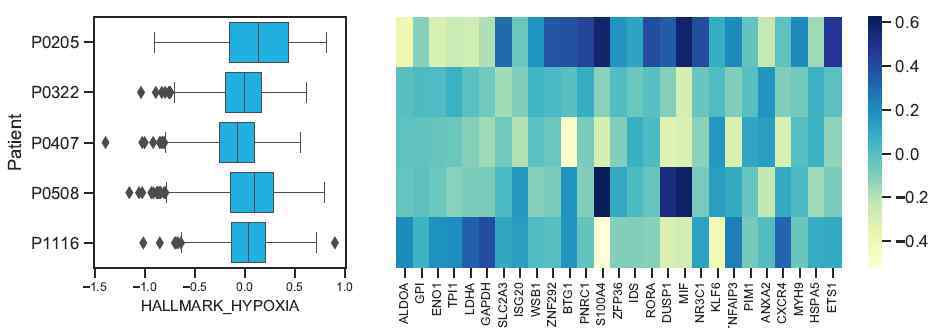
患者间代谢特征差异分析

单细胞基因表达的驱动因素分析
以上图片均来自郝波生物
郝波生物学十周年
福利一
凭借六年的经验,郝波生物基于SMART-seq技术为人类、小鼠、大鼠、果蝇、斑马鱼、牛、羊和其他物种的样本提供单细胞测序服务。研究结果发表在《细胞研究》、《自然神经病学》等期刊上。最近,郝波生物的单细胞测序平台增加了一项新技术——BD Rhapsody,可以提供更大、更灵活、更全面的单细胞测序服务。
福利二
郝波学院-国家自然培训课程,大咖啡为您提供一对一的回答服务。在拒绝倾听的时候,忽悠一下训练模式,忽悠一下我们所做的事情的内涵和灵魂是有用的!现在注册获取2018年国家自然申请空的白色模板,我们将直接发送到您的电子邮件地址。
福利三
送祝福,收礼物!丁当,36 G知识包u盘,mi乐队,SCI高分文章包,新秀丽行李箱等。,请点击“阅读原文”接受礼物!
2018年12月15日,郝波生物将在上海举办第四届生物标志物及临床应用研讨会,恰逢郝波成立10周年。欢迎大家分享!
引用
[1]唐芳,巴巴多斯,王勇,诺德曼,李春,等.单个细胞的基因全序列分析.Nat方法2009,6(5):377-382。
单细胞RNA序列揭示哺乳动物细胞中动态、随机的单等位基因表达。科学,343(6167):193-196。
[3]德索萨n .单细胞遗传学。Nat方法2013,10(9):820。
[4]基因组生物学。单细胞测序解决基础和生物医学问题。理科2012,336(6084):976-7。
[5]2013年度最佳方法。Nat方法2014,11(1):1。
[6]唐F,老K,苏拉尼马。单细胞染色体分析的发展和应用自然方法2011,8(4补充):S6-11。
[7]史密斯c .巨蟹座通过多样性显示实力。Nature 2013,499(7459):505-8。
循环肿瘤细胞:分离和分析的进展,以及临床应用的挑战。药典2014,141(2):209-21。
[9]洛瓦特,卢布,李,杜克,金,等。活体组织中空间定义单细胞的体内分析(TIVA)。Nat方法2014,11(2):190-196。
[10]佐佐川Y,二阶堂一,早矢T,丹诺H,宇野KD,等。石英-Seq:一种高度可重复和敏感的单细胞RNA测序方法,揭示了非遗传基因表达的异质性。基因组Biol 2013,14(4):R31。
[11]伊斯拉姆·S1,基尔奎斯特,莫里纳·阿,·P,范杰布,等.用高度多重RNA序列表征单细胞传统景观.基因组Res 2011,21(7):1160-7。
[12]等.单细胞水平的RNA和单个循环肿瘤细胞全长基因序列.Nat Biotechnol 2012,30(8):777-782。
[13]皮塞利,法利达尼或,比约克隆德AK,温伯格G,萨格瑟S,等。全长RNA-序列从单细胞使用智能seq2。Nat协议2014,9(1):171-81。
[14] Patel AP,Tirosh I,特隆贝塔JJ,Shalek AK,Gillespie SM,等.单细胞RNA-seq强调了原发性胶质母细胞瘤的瘤内异质性.科学2014,344(6190):1396-401。
[15]蒂罗什I,伊扎尔B,普拉卡丹SM,沃兹沃斯MH,特拉塞D,等.用单细胞RNA-seq解剖转移性黑色素瘤的多细胞生态系统.《科学》2016,352(6282):189-96。
[16] Grün D,Lyubimova A,Kester L,Wiebrands K,Basak O,等.单细胞信使RNA测序揭示罕见的肠细胞类型。Nature 2015,525(7568):251-5。
[17]李·麦克,洛佩兹-迪亚兹·FJ,汗·西,塔里克·马,戴恩·尤,等.通过RNA测序对癌细胞耐药性转变过程中的异质性进行单细胞分析.美国国家科学院学报2014,111(44):E4726-35。
[18]Kim KT,Lee HW,Lee HO,Kim SC,Seo YJ,等。单细胞基因测序鉴定肺腺癌细胞抗癌药物反应的亚克隆异质性。基因组生物2015,16:127。
[19] Miyamoto DT,Zheng Y,Wittner BS,Lee,Zhu H,等.单个前列腺癌CTCs的RNA-Seq在抗雄激素抵抗中暗示非匿名Wnt信号.理科2015,349(6254):1351-6。
[20]郑c,郑l,柳建康,等.单细胞测序揭示肝癌浸润性T细胞的景观.单元格2017,169(7):1342-1356。
[21]郭x,张勇,郑力,等.非小细胞肺癌T细胞的单细胞测序全局表征.Nat Med 2018,24(7):978-985。
[22]李力,董军,严力,等.单细胞RNA-Seq分析绘制人类生殖系细胞发育和性腺生态位相互作用图.细胞干细胞2017,20(6):858-873。
[23]李CL,李KC,吴d,等.高覆盖率单细胞RNA测序鉴定体感神经元类型及功能异质性.细胞研究2015,26(1):83-102。
[24]麦考利集成电路,哈尔蒂,库马尔,等。T-seq:单细胞基因组和染色体的平行测序。自然方法2015,12(6): 519-522。
[25] Angermueller C,Clark SJ,Lee HJ,Macaulay IC,Teng MJ,等. Rek平行单细胞测序连接传统和表观遗传异质性.Nat方法2016,13(3):229-32。
[26]胡勇,黄k,安青,杜刚,胡刚,等.单细胞染色体和DNA甲基体的同时分析.基因组生物2016,17:88。
[27]侯勇,郭浩,曹c,李x,胡斌,等.单细胞三组学测序揭示肝细胞癌的遗传,表观遗传和染色体异质性.细胞研究2016,26(3):304-19。
[28] Macosko EZ,Basu A,Satija R,Nemesh J,Shekhar K,等.使用纳升液滴的单个细胞的高度平行全基因组表达谱。单元格2015,161(5):1202-14。
[29] Klein AM,Mazutis L,Akartuna I,Tallapragada N,Veres A,等.单细胞组学的液滴条形码应用于胚胎干细胞。单元格2015,161(5):1187-201。
[30]M . Soumillon,D . Cacchiarelli,S . SEM RAU,等.高通量单细胞RNA-Seq定向分化的特征.解剖记录2014,217(1):16
[31]樊HC1,傅GK1,。表达式分析。用于基因表达细胞术的单细胞组合标记。理科2015,347(6222):1258367。
[32]郑,特里,贝尔平地机P,瑞夫金P,本特ZW,等.单细胞大规模并行数字图谱.Nat Commun 2017,8:14049。
[33]罗森伯格,洛可厘米,马斯喀特拉,库奇纳,样本P,等。发育中的小鼠大脑和脊髓的单细胞谱与分裂池条形码。《科学》2018,360(6385):176-182。
标题图来源:酷罗海站
1.《火炎 单细胞测序,到底为什么这么火炎焱?!》援引自互联网,旨在传递更多网络信息知识,仅代表作者本人观点,与本网站无关,侵删请联系页脚下方联系方式。
2.《火炎 单细胞测序,到底为什么这么火炎焱?!》仅供读者参考,本网站未对该内容进行证实,对其原创性、真实性、完整性、及时性不作任何保证。
3.文章转载时请保留本站内容来源地址,https://www.lu-xu.com/guoji/767695.html